Le cerveau en lumière
Une technique innovante, baptisée "optogénétique", permet de contrôler des cellules cérébrales par la lumière. Ouvrant des perspectives infinies pour la recherche en neurobiologie, notamment sur les maladies de Parkinson.
Par La rédaction d'Allo Docteurs
Rédigé le
La prestigieuse revue Nature Methods l’a consacrée "Méthode de l’année 2010". Et plus de 800 laboratoires de recherche y ont désormais recours. L’optogénétique combine les outils de l’optique à ceux de la génétique. Elle consiste à contrôler certaines cellules par la lumière en y insérant au préalable une protéine spécifique. La lumière, bleue en l’occurrence, joue le rôle d’un interrupteur : présente, elle active la cellule ; absente, elle la désactive. "Cette méthode est en train de changer l’horizon de la neurobiologie", s’enthousiasme Valentina Emiliani, chercheuse au CNRS.
Tout commence par un mystère. En 2002, un biologiste allemand, Peter Hegemann, tente de comprendre pourquoi une algue au nom barbare, Chlamydomonas Renhardtii, se déplace en fonction de la lumière : mobile le jour, elle est immobile la nuit. Il découvre que cette algue contient une protéine sensible à la lumière bleue. En présence de lumière, cette protéine active des charges électriques positives dans l’algue et entraine son mouvement. Sans lumière, l’algue ne bouge plus.
Partant de cette découverte, des chercheurs ont eu l’idée d’introduire cette protéine dans des cellules du cerveau, afin de contrôler leur activité par la lumière. La méthode est simple : via un virus, on introduit dans le groupe de neurones choisi les gènes responsables de la fabrication de cette protéine.
"C’est une révolution technique", explique Pierre-Marie Lledo, chercheur à l’Institut Pasteur. "On peut désormais activer spécifiquement des populations de cellules bien précises". En effet, la lumière bleue va activer uniquement la cellule contenant la protéine, et non le neurone voisin. Un grand pas par rapport aux précédentes techniques : "Les impulsions électriques envoyées via des électrodes, par exemple, avaient un impact sur toute une zone, et ne permettaient pas de contrôler spécifiquement certaines cellules. C’est donc un changement considérable dans l’outil utilisé : d’une grosse masse, on passe à un scalpel".
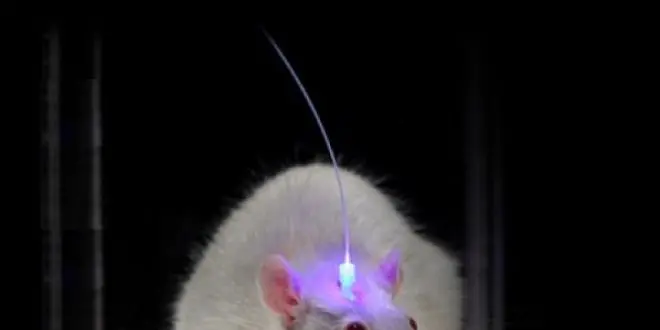
Pierre-Marie Lledo, dont les recherches portent sur les activités des néo-neurones, qui naissent dans le cerveau adulte, utilise donc cet "outil de choix" pour stimuler spécifiquement les néo-neurones et comprendre leur fonction. Par des fibres optiques, il stimule dans le cerveau de certaines souris ces néo-neurones et s’est rendu compte qu’elles jouaient un rôle dans l’apprentissage.
Autre exemple : une étude a permis de neutraliser par la lumière les neurones responsables de la motricité, et donc du mouvement. C’est ce qu’on peut voir sur cette étonnante vidéo d’une souris dont le mouvement circulaire s’arrête soudainement, quand il n’y a plus de faisceau lumineux.
L’expérience a été réitérée sur des souris parkinsoniennes par une équipe de l’université de Stanford. Elle a réussi à identifier très précisément les neurones à neutraliser pour faire régresser les symptômes moteurs de la maladie de Parkinson.
L’optogénétique ouvre donc des perspectives sans fin pour la recherche, permettant d’étudier très précisément le rôle de tel ou tel groupe de neurones – et éventuellement agir dessus.
Pour en savoir plus :