Ebola : tout savoir sur les traitements potentiels
Aucun traitement n'a encore confirmé son efficacité contre les infections humaines du virus Ebola. Toutefois, des combinaisons de médicaments ont déjà été testées sur des personnes contaminées, certaines d'entre elles ayant été guéries. Si la diversité des cas (traitement peu de temps après l'infection ou après apparition des symptômes) rend difficile leur analyse, plusieurs résultats récents invitent à l'optimisme.
Par La rédaction d'Allo Docteurs
Rédigé le

Le Zmapp
Le ZMapp est un cocktail d'anticorps produits en laboratoire, développé par la société Mapp Bio. Il s'agit donc d'un "sérum artificiel". Les anticorps utilisés sont une duplication à l'identique, et en grande quantité, d'anticorps produits par des souris infectées par le virus, et modifiés par génie génétique pour maximiser leur efficacité chez l'humain.
Comment le ZMapp agit-il ?
Les anticorps empêchent les virus de se fixer aux cellules, et donc de les infecter. Les virus ne pouvant se dupliquer qu'après avoir infecté les cellules, ils ne peuvent plus proliférer dans l'organisme, et l'infection peut être endiguée par le système immunitaire.
Quelle efficacité potentielle sur l'homme ?
Ce médicament expérimental a montré de très bons résultats dans des expérimentations sur le singe.
Sans avoir fait l'objet d'essais cliniques, il a déjà été administré "à titre compassionnel" à plusieurs patients infectés par le virus Ebola.
Mi-septembre, sept malades humains avaient reçu le traitement, cinq d'entre-eux ont survécu. Toutefois, peu d'informations sont disponibles sur les autres médicaments reçus, dans le même temps, par les malades. Le Dr Kent Brantly, 33 ans, l'un des premiers bénéficiaires du Zmapp (aujourd'hui guéri) a également reçu le TKM-Ebola. L'efficacité propre du sérum reste donc à établir.
Un prêtre espagnol de 75 ans et un médecin libérien qui avaient également reçu ce médicament sont en revanche décédés.
Mi-septembre, le professeur Jean-François Delfraissy, directeur de l'Institut de microbiologie et des maladies infectieuses (IMMI), expliquait que les stocks disponibles de Zmapp étaient, pour l'heure, très réduits.
La Norvège, où vient d'être rapatriée une femme médecin de MSF, contaminée en Sierra Leone, est en passe de se procurer "la dernière dose actuellement disponible", selon un haut responsable des autorités pharmaceutiques norvégiennes, Steinart Madsen. Selon Mapp Bio, "quelques centaines de doses" devraient être disponibles d'ici la fin de l'année. La production du traitement resterait toutefois lente, et très coûteuse.
L'Avigan®

Comprimés d'Avigan® (DR)
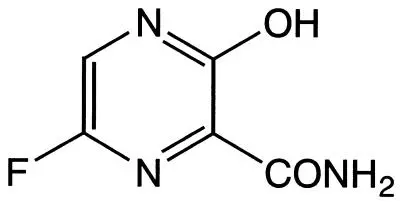
Représentation de la molécule favipiravir
L'Avigan® est un médicament antiviral homologué en mars 2014 au Japon pour le traitement de la grippe. Se présentant sous forme de comprimés, il serait - s'il s'avérait efficace contre Ebola - plus simple d'utilisation en zone d'intervention que d'autres traitements injectables
Comment l'Avigan® agit-il ?
La molécule active de l'Avigan®, le favipiravir (T-705), est étudiée depuis le début des années 2000. Elle a démontré une certaine efficacité contre la prolifération de divers virus (souches de la grippe, fièvre jaune, fièvre aphteuse…). Selon les données disponibles, la molécule agit en empêchant la réplication du matériel génétique du virus.
Deux études menées sur la souris, publiées en avril et en mai 2014, ont révélé l'efficacité potentielle du favipiravir pour prévenir l'infection par une souche du virus Ebola, et le traitement de cette infection "au moins jusqu'à six jours après contamination". Chez la souris, les premiers symptômes de la maladie peuvent être détectés trois jours après l'infection.
Quelle efficacité potentielle sur l'homme ?
L'Avigan® a fait parti de l'un des deux traitements administrés à l'infirmière française de MSF (aujourd'hui guérie), selon un communiqué diffusé fin septembre par la société Toyama Chemical (filiale de FujiFilm), titulaire des brevets sur le favipiravir. Pour l'heure, il n'est pas possible de déterminer dans quelle mesure ce médicament a contribué à la guérison de la malade.
Un médecin rapatrié à Francfort après avoir contracté la fièvre Ebola au Sierra Leone serait actuellement traité par Avigan®, selon la même source.
Fin août, le groupe Toyama Chemical avait annoncé disposé de réserves de traitement "pour 20.000 personnes".
Un essai pour évaluer l'efficacité de ce composé à plus grande échelle devrait démarrer en novembre en Guinée, et concernerait environ 80 malades.
Le TKM-Ebola
Le TKM-Ebola (ou TKM-100-802) est un traitement expérimental développé par la société canadienne Tekmira (TKM) Pharmaceuticals.
Comment le TKM-Ebola agit-il ?
Selon les données disponibles, le TKM-Ebola cible les chaînes de molécules qui transcrivent le code génétique du virus (et qui sont normalement ultérieurement transcrites dans les cellules infectées pour synthétiser de nouvelles copies du virus).
Les essais cliniques sur personnes saines (destinées à évaluer la tolérance et l'absence d'effets indésirables du traitement) ont débuté en janvier 2014. Sans attendre les résultats de ces recherches, le CDC (Centre pour la prévention et le contrôle des maladies des Etats-Unis) a autorisé cet été l'utilisation expérimentale du TKM-Ebola en cas d'urgence.
Quelle efficacité potentielle sur l'homme ?
Le TKM-Ebola a fait partie des médicaments utilisés pour traiter le docteur Kent Brantly, soigné le mois dernier dans un hôpital d'Atlanta, et aujourd'hui guéri.
Le 30 septembre, le CDC a annoncé que le TKM-Ebola ferait parti des traitements potentiellement utilisés pour traiter Thomas Duncan, le patient hospitalisé au Texas suite à une infection à Ebola survenue au Libéria. Seul le brincidofovir (produit par la société Chimerix, voir ci-après) aurait toutefois été utilisé sur le malade, décédé le 8 octobre 2014.
Selon l'OMS, 900 traitements TKM-Ebola pourraient être mis à disposition par Tekmira d'ici début 2015.
Le brincidofovir
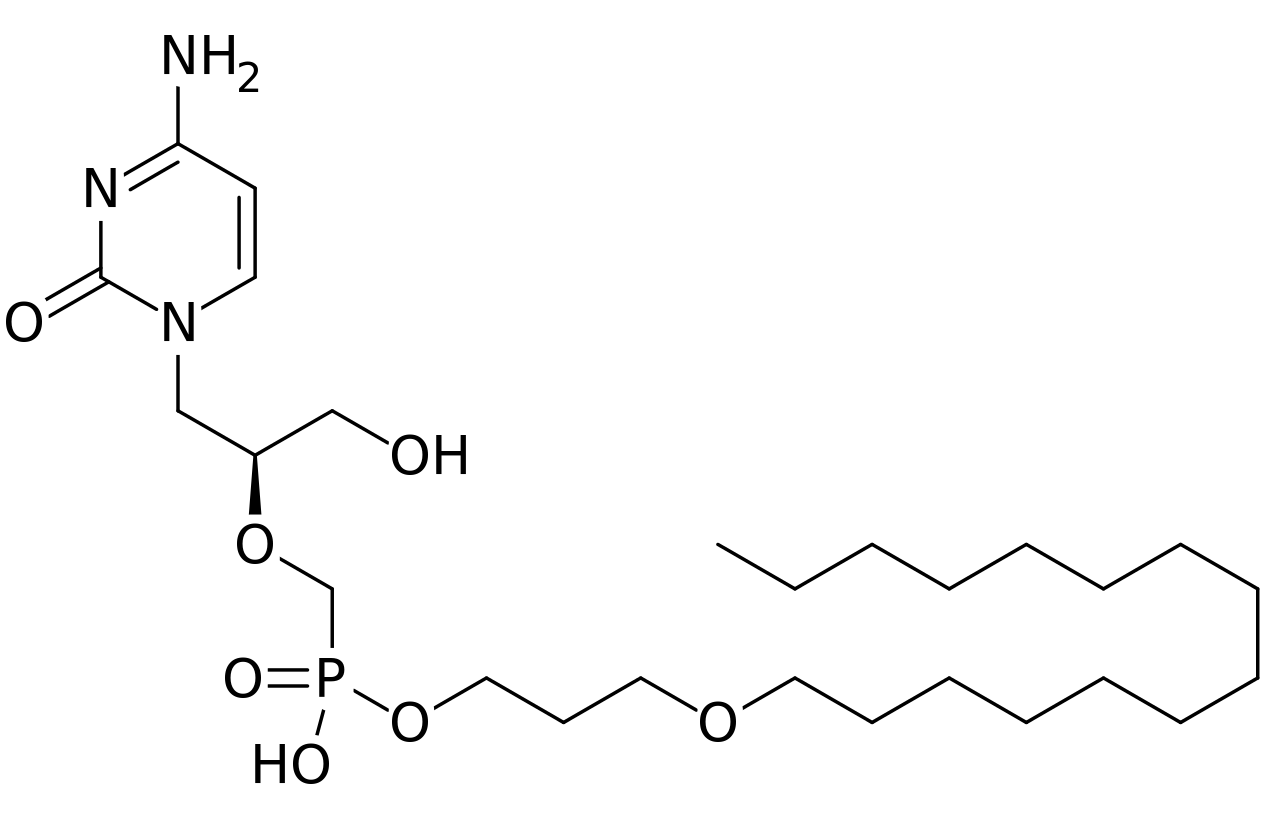
Le brincidofovir (CMX001) est antiviral administrable par voie orale, développé par la firme américaine Chimerix pour lutter contre d'autres virus (adénovirus et cytomégalovirus).
Il fait actuellement l'objet d'un essai de phase III (dernière étape avant une demande de commercialisation) contre ces autres virus, précise la firme. Au total, mille personnes ont reçu cet antiviral. Il possède une importante nephrotoxicité (dommages causés aux reins).
Comment agit-il ?
La molécule est incorporée par les cellules infectée, et sert de "cheval de Troie" à un composé du nom de cidofovir. Celui-ci empêche la réplication des virus dont le matériel génétique est constitué d'ADN en empêchant la transcription de cet ADN par la cellule.
Si les virus responsables de la fièvre Ebola sont des virus à ARN (et non à ADN), la firme qui produit le médicament a annoncé début septembre qu'il présentait, in vitro, "des signes d'activité" contre Ebola.
Quelle efficacité potentielle sur l'homme ?
Thomas Duncan, le patient hospitalisé au Texas suite à un séjour au Libéria, est le premier patient atteint d'Ebola à recevoir cette molécule. Il est décédé le 8 octobre.
Autres thérapies expérimentales
De nombreuses autres thérapies expérimentales sont en cours de développement, et font l'objet d'une véritable course entre laboratoires pharmaceutiques. Parmi eux, il faut citer :
La lamivudine, molécule antivirale disponible en Afrique dans le cadre de la lutte contre l'épidémie de sida, aurait par ailleurs été utilisée par un médecin libérien pour soigner une quinzaine de personnes, selon des reporters de CNN. Cette thérapie, utilisée en désespoir de cause, aurait selon lui permis de traiter efficacement "treize des quinze malades". L'Institut national américain des allergies et des maladies infectieuses aurait pris contact avec le médecin en vue de mettre en place un protocole d'essai au Libéria.
L'utilisation de thérapies à base de sang de personnes guéries (comme les sérums de convalescents), dans les pays affectés, représente une autre option. L'idée est ici de transmettre des anticorps pouvant bloquer la prolifération du virus à des patients qui n'ont pas pu développer une telle immunité. "La transfusion de sang a démarré, à petite échelle", a récemment indiqué Marie-Paule Kieny, sous-directeur général de l'OMS, précisant que le nombre de transfusions pratiquées sur des malades d'Ebola devrait augmenter "au début de l'année prochaine".
Lors de contamination accidentelle en laboratoire, des procédures d'urgences peuvent être mise en œuvre dans les secondes qui suivent pour essayer de faire barrage à l'infection (drainage sanguin). Ces protocoles (et les "guérisons d'Ebola" associées décrites dans les annales médicales) ne peuvent malheureusement pas constituer un traitement après apparition des symptômes.
Des thérapies préventives ?
L'Organisation mondiale de la santé (OMS) a récemment fait état de deux candidats vaccins "prometteurs" :
L'OMS espère de premiers résultats des essais sur ces deux vaccins en novembre-décembre et le début d'essais de phase 2 (permettant d'évaluer l'efficacité du vaccin) dans les pays touchés dès janvier-février.
Par ailleurs, la firme Johnson & Johnson a récemment annoncé l'accélération du développement d'un vaccin utilisant la technologie d'une société de son groupe, Crucell N.V., et celle d'une société de biotechnologie basée au Danemark, Bavarian Nordic.
Début octobre, la société Inovio, qui développe un vaccin contre Ebola depuis quelques années, a pour sa part affirmé avoir obtenu des résultats concluants sur l'animal. Des essais cliniques sur l'humain ont été annoncés pour le début de l'année 2015.
En savoir plus sur les traitements potentiels contre le virus Ebola :