DMLA : la France toujours privée d'un traitement peu coûteux et efficace
Pourquoi l'Avastin®, traitement anti-cancéreux ayant démontré son efficacité pour traiter la dégénérescence maculaire liée à l'âge (DMLA) n'est-il toujours pas autorisé en France pour cette indication ? François Chast, chef du service pharmacie à l'hôpital Cochin-Hôtel-Dieu (Paris), était l'invité du Magazine de la Santé du 5 février 2014 pour faire un point sur cette affaire...
Par La rédaction d'Allo Docteurs
Rédigé le
Depuis 2012, la polémique enfle autour du laboratoire Roche qui refuse de demander l’autorisation de mise sur le marché français d’un traitement de la DMLA (dégénérescence maculaire liée à l'âge), efficace et bon marché. La raison de ce refus serait exclusivement financière : en effet, le laboratoire reçoit de substantielles royalties de la part de Novartis, qui commercialise le Lucentis®, un traitement 20 à 40 fois plus cher initialement créé par Genentech... une filiale de Roche.
Six études successives(1) ont révélé puis confirmé que les deux traitements sont également efficaces. Ils ne se différencient pas non plus en matière d'effets secondaires…
En France, l'Avastin® est autorisé en cancérologie(2) comme anti-angiogènique (c’est-à-dire qu'il empêche la formation de vaisseaux sanguins irriguant les tumeurs). Fin juillet 2012, alors que des premiers travaux avaient démontré l'intérêt de l'Avastin® pour le traitement de la DMLA, la Direction générale de la santé (DGS) a demandé aux agences régionales de santé (ARS) d'interdire formellement son usage dans ce contexte. Une décision qui a déclenché les foudres de nombreux ophtalmologistes et économistes.
Mais voilà : sans demande d'AMM spécifique par Roche, le dossier ne pouvait, en théorie, pas évoluer. Pourtant, en décembre 2012, un texte voté au parlement a autorisé la création de "recommandations temporaires d'utilisations pour raisons économiques" - un dispositif qui permet d'élargir sans délai, pour des raisons financières, les applications autorisées d'un médicament disposant déjà d'une AMM. Cependant, à ce jour, aucun décret d'application n'a encore été signé pour ce texte.
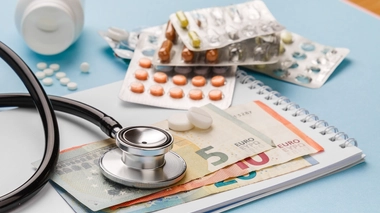
Le Lucentis® des laboratoires Novartis, en vente depuis 2006, coûte 800 euros la dose, contre 30 à 50 euros pour l'Avastin®, au dosage efficace(3) pour la DMLA. L'utilisation de l'Avastin® pourrait permettre une économie annuelle de plus 200 millions d'euros à la Sécurité sociale.
---
(1) La dernière en date : Ranibizumab versus Bevacizumab for Neovascular Age-related Macular Degeneration: Results from the GEFAL Noninferiority Randomized Trial. L. Kodjikian et coll. Ophthalmology. nov. 2013, publié en ligne en août 2013. doi:10.1016/j.ophtha.2013.06.020 (les résultats de ces travaux avaient été présenté en mai 2013 à l’occasion du congrès mondial d’Ophtalmologie de Seattle).
(2) Le rapport bénéfice/risque de l'Avastin® en cancérologie fait actuellement l'objet d'un vif débat. Ce dernier ne concerne pas l'intérêt thérapeutique du médicament pour la DMLA.
(3) Un laboratoire allemand, Apozyt, commercialise l’Avastin® en Europe en le reconditionnant aux doses efficaces pour le traitement de la DMLA. Début 2013, Novartis avait attaqué le laboratoire pour concurrence déloyale devant la Cour européenne, mais avait été débouté.
VOIR AUSSI :
Il existe deux formes de DMLA. L'une dite "sèche", qui ne dispose pas de traitement, et une forme "humide", qui se soigne par une injection dans l'œil une fois par mois.