Leucémie myéloïde chronique : un antidiabétique pour guérir certains patients
En utilisant certaines propriétés chimiques d'un médicament anti-diabétique connu (la pioglitazone), des chercheurs français et étasuniens semblent être parvenus à guérir plusieurs patients atteints d'un cancer rare du sang. Leurs travaux ont été publiés ce 2 septembre 2015, dans la prestigieuse revue Nature.
Rédigé le , mis à jour le
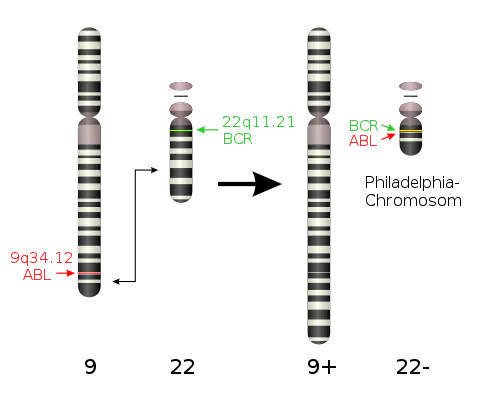
Représentation schématique de la formation du chromosome de Philadelphie (cc-by-sa Obeidat / Uegly).
La leucémie myéloïde chronique (LMC) est un cancer du sang rare, puisque moins de 700 nouveaux cas se déclarent annuellement en France, principalement des adultes âgés de 30 et 50 ans. Ce cancer est caractérisé par une production anormale de globules blancs par la moelle osseuse (essentiellement des globules blancs neutrophiles, mais également des éosinophiles et des basophiles, et un grand nombre de cellules immatures). Elle évolue presque toujours vers une leucémie aiguë.
Depuis le début des années 2000, des traitements permettent de freiner la croissance des cellules cancéreuses, et de diminuer leur prolifération dans le sang. Le principal représentant de ces médicaments est l'imatinib mésylate (Glivec®)[1], qui court-circuite l'action de plusieurs tyrosines kinases (facteurs de croissance cellulaires) en prenant leur place sur les récepteurs situés à la surface ou au cœur des cellules – ici, dans les globules blancs (voir encadré). Mais dans 75% à 90% des cas, ce traitement ne fait que juguler la maladie : les cellules souches qui produisent les globules blanc en trop grande quantité restent actives, et continuent à en inonder le corps.
En 2009, des chercheurs nord-américains avaient révélé que la survie de nombreuses cellules souches dépendait de la présence d’une protéine nommée STAT5. L’année suivante, une autre équipe découvraient que la survie des cellules souches responsables de la LMC requerrait des taux anormalement élevés de cette protéine.
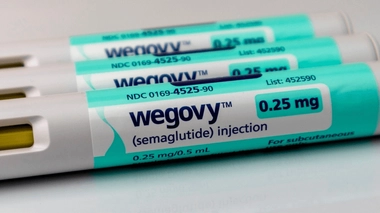
Or, dès 2008, des chercheurs français avaient établi que l’activation d’un récepteur cellulaire entraînait une réduction drastique de la production de STAT5. Forts des découvertes réalisées ultérieurement, ces scientifiques ont cherché à identifier une molécule capable d’activer ce fameux récepteur. Et leurs efforts ont payé : ils s’agit de la pioglitazone, un traitement anti-diabétique oral retiré du marché français en 2011[2] suite à des signalements de pharmacovigilance. En cas de prise prolongée, cette molécule entraînait un risque accru de cancer de la vessie.
Mais les chercheurs ne souhaitaient l’employer qu’à faibles doses, et dans un contexte thérapeutique précis. Les chercheurs ont recruté quelques patients souffrant de LMC et de diabète de type II, pour réaliser un essai clinique. Selon les données publiées ce 2 septembre 2015, dans la revue Nature, ces patients traités avec ces deux médicaments ne présentaient plus de signe de LMC (ce qui reste vrai après bientôt cinq années de suivi post-traitement).
L’expérience a ensuite été réitérée sur 24 patients non diabétiques. Un traitement de douze mois combinant imatinib et pioglitazone a entraîné la rémission de plus de la moitié d’entre eux (contre seulement un quart d’un groupe témoin uniquement traité par imatinib).
Les propriétés chimiques de la pioglitazone sont désormais bien connues. Les chercheurs concluent que "le simple ajout [de ce médicament] apporte de l’espoir pour éradiquer complètement la LMC chez de nombreux patients."
Source : Erosion of the chronic myeloid leukaemia stem cell pool by PPAR-gamma agonists. S.Prost et coll. Nature, 2 sept. 2015.
[nextpage]
[1] D’autres molécules (dasatinib, nilotinib) ont vu le jour à destination des patients tolérant mal l'imatinib mésylate, ou développant des résistances.
[2] Autrefois commercialisée en France sous le nom d'Actos® (et, en association avec une autre molécule, sous-celui de Competact®), elle reste autorisée dans de nombreux pays.
La leucémie myéloïde chronique découle d’un échange de matériel génétique entre les 9ème et 22ème chromosomes de certaines cellules souches (formation du "chromosome de Philadelphie"). Cette fusion entraîne la formation d’un gène, BCR-ABL, codant pour une enzyme (une tyrosine kinase) qui stimule la production de globules blancs (voir illustration ci-dessous).